ORYZON anuncia sus resultados y avances en el primer trimestre de 2026
- Las inversiones en I+D alcanzan los 4,5 M€, lo que supone un incremento del 88% (2,1 M€) respecto a los 2,4 M€ invertidos en el mismo periodo del ejercicio precedente
- El resultado neto de 1,2 M€ de pérdida mejora en 0,5M€ con respecto al primer trimestre del ejercicio 2025
- Al cierre del primer trimestre de 2026 el efectivo y las inversiones financieras disponibles ascienden a 22,1 M€
- Se presentarán datos positivos actualizados de iadademstat en pacientes con LMA en 1L en EHA, con 100% de respuestas (ORR), un 93% de tasa de respuestas completas compuesta (RCc) y un 79% de RC estrictas a la fecha de corte de datos para el abstract
- También se presentarán en EHA datos positivos actualizados de iadademstat en LMA FLT3 mutada en recaída/refractaria, con una RCc del 67%
MADRID, ESPAÑA y CAMBRIDGE, EE.UU., 14 de mayo de 2026 – Oryzon Genomics S.A., compañía biofarmacéutica de fase clínica y líder global en epigenética, ha anunciado hoy sus resultados y avances en el primer trimestre de 2026.
“Durante los primeros meses de 2026, Oryzon ha seguido impulsando sus franquicias de oncología/hematología y de SNC, manteniendo al mismo tiempo una sólida posición financiera”, ha comentado el Dr. Carlos Buesa, CEO de Oryzon. “Especialmente relevante es que iadademstat continúa generando datos clínicos muy alentadores en leucemia mieloide aguda, reforzando aún más nuestra convicción sobre el potencial terapéutico diferencial del compuesto y su oportunidad comercial.”
“Estamos especialmente entusiasmados con las próximas presentaciones en EHA 2026, donde se presentarán resultados actualizados de seguridad y eficacia de los estudios ALICE-2 y FRIDA”, ha añadido el Dr. Buesa. “En LMA de primera línea, la combinación triple de iadademstat con azacitidina y venetoclax continúa mostrando un perfil de eficacia altamente competitivo, que creemos se compara muy favorablemente con otros regímenes triples emergentes en este campo. En EHA presentaremos datos actualizados de 18 pacientes, incluyendo actividad alentadora en pacientes con perfiles genéticos adversos. Sobre la base de los avances alcanzados hasta la fecha, creemos que las combinaciones basadas en iadademstat pueden representar una oportunidad diferenciada y competitiva para un desarrollo clínico acelerado en LMA de primera línea y podrían respaldar el avance hacia un programa de Fase II/III potencialmente pivotal con el objetivo de obtener una aprobación regulatoria acelerada.”
“El desarrollo clínico de iadademstat continúa expandiéndose, reforzando su potencial como un activo de alto valor en hematología y oncología”, ha continuado el Dr. Buesa. “El reclutamiento de pacientes sigue avanzando en múltiples estudios promovidos por investigadores en destacados centros oncológicos de EE.UU. o esponsorizados por el National Cancer Institute en neoplasias hematológicas y tumores sólidos. Al mismo tiempo, las oportunidades emergentes en hematología no oncológica, incluyendo la anemia de células falciformes y la trombocitemia esencial, podrían ampliar de manera significativa el alcance comercial y estratégico de la franquicia. En conjunto, creemos que iadademstat generará catalizadores clínicos cada vez más diversificados y producirá un flujo continuado de datos, respaldando un sólido ritmo de noticias y avances en los próximos trimestres.”
“En SNC, seguimos plenamente comprometidos con el avance de vafidemstat hacia etapas avanzadas de desarrollo clínico”, ha comentado el Dr. Buesa. “Seguimos progresando en las actividades necesarias para respaldar la nueva presentación del protocolo de Fase III PORTICO-2 tras los comentarios recibidos de la FDA, al tiempo que avanzamos en el estudio EVOLUTION en esquizofrenia y en los preparativos del nuevo estudio HOPE-2 en trastorno del espectro autista. Creemos que vafidemstat continúa representando un importante generador de valor a largo plazo para Oryzon.”
EVOLUCIÓN DEL NEGOCIO
Primer trimestre y otros destacados recientes
Iadademstat:
- Oryzon anunció la aceptación para presentación en el Congreso de la European Hematology Association (EHA) 2026 de datos positivos actualizados del ensayo clínico de Fase Ib ALICE-2 en curso con iadademstat en combinación con venetoclax y azacitidina en pacientes con leucemia mieloide aguda (LMA) de nuevo diagnóstico. A la fecha de corte de datos para el abstract de febrero de 2026, la combinación triple continuó mostrando un perfil de seguridad favorable y elevadas tasas de respuesta. Entre los pacientes evaluables (n=14/15), la tasa de respuesta global (ORR) fue del 100% (14/14), con una tasa de respuesta completa (RC) del 79% (11/14) y una tasa de remisión completa compuesta (RCc: RC+RCh+RCi) del 93% (13/14). Tras una mediana de seguimiento de 6 meses, la tasa estimada de supervivencia global a 12 meses fue del 74%. Datos actualizados con pacientes adicionales y respuestas más maduras serán presentados en EHA en junio de 2026. Este estudio promovido por investigadores (IIS) está liderado por el Knight Cancer Institute de Oregon Health & Science University (OHSU) y prevé reclutar hasta 24 pacientes para alcanzar 21 pacientes evaluables. El ensayo continúa reclutando pacientes activamente.
- Datos positivos actualizados del ensayo clínico de Fase Ib FRIDA en curso, y con el reclutamiento completado, de iadademstat en combinación con gilteritinib en pacientes con LMA con mutación FLT3 en recaída o refractaria (R/R) también han sido aceptados para su presentación en EHA 2026. Los datos actualizados de la cohorte de expansión mostraron un perfil de seguridad favorable y una tasa de RCc del 67% (12/18 pacientes evaluables para respuesta con mutaciones FLT3 canónicas) en una población de pacientes intensamente pretratada. Estos resultados se comparan favorablemente con las respuestas observadas con gilteritinib en monoterapia en cohortes contemporáneas de práctica clínica real enriquecidas con pacientes intensamente pretratados, en las que se ha reportado una tasa de RC+RCi del 28%. Durante el congreso se presentarán datos adicionales del estudio.
- Se ha iniciado el reclutamiento de pacientes en un nuevo ensayo de Fase Ib de iadademstat en combinación con un inhibidor de puntos de control inmunitarios y radioterapia en cáncer de pulmón de células pequeñas en estadio extenso (CPCP-EE), esponsorizado por la Universidad de Yale. El estudio evalúa iadademstat en combinación con atezolizumab y radioterapia corporal estereotáctica (SBRT), seguido de terapia de mantenimiento con atezolizumab e iadademstat, en pacientes con CPCP-EE residual, progresivo o recurrente que previamente recibieron quimioterapia basada en platino, con o sin tratamiento con inhibidores de puntos de control inmunitario.
- El reclutamiento de pacientes ha continuado en otros estudios clínicos en curso con iadademstat, realizados en el marco del Acuerdo de Investigación y Desarrollo Cooperativo (CRADA, por sus siglas en inglés) con el National Cancer Institute (NCI) de EE.UU. en LMA de primera línea, neoplasias mieloproliferativas y CPCP, así como en un estudio promovido por investigador en síndrome mielodisplásico.
- Oryzon continúa avanzando en el ensayo de Fase Ib RESTORE de iadademstat en pacientes adultos con anemia de células falciformes (ACF). El estudio evaluará la seguridad y tolerabilidad de iadademstat, establecerá la dosis recomendada para Fase II (RP2D) e investigará el efecto de iadademstat sobre la inducción de la expresión de hemoglobina fetal (HbF), un criterio de valoración clínicamente relevante en ACF. El ensayo continúa reclutando pacientes activamente y la Compañía espera comunicar las primeras actualizaciones clínicas antes de final de año.
- Oryzon ha recibido autorización regulatoria de la Agencia Europea de Medicamentos (EMA) para iniciar el ensayo de Fase II IDEAL, que evaluará iadademstat en pacientes adultos con trombocitemia esencial (TE) resistentes o intolerantes a hidroxiurea. Las actividades de activación de los centros participantes y los preparativos para el inicio del estudio están en curso.
- Oryzon ha continuado reforzando su cartera de patentes para iadademstat. La Oficina de Patentes y Marcas de Estados Unidos (USPTO) ha concedido recientemente una patente que cubre métodos para el tratamiento de enfermedades neoplásicas con combinaciones que incluyen iadademstat y otros agentes terapéuticos, en particular venetoclax. Se espera que la patente permanezca en vigor hasta enero de 2039, incluyendo 681 días de ajuste del plazo de patente (PTA, por sus siglas en inglés), excluyendo cualquier posible extensión de la duración de la patente relacionada con la revisión regulatoria. Se han concedido patentes que cubren combinaciones de iadademstat con venetoclax también en Australia, Brasil, Canadá, Europa, India, Israel, Japón, Corea, Malasia, México, Nueva Zelanda y Rusia. Además, Oryzon ha recibido recientemente una comunicación de “Decisión de concesión” por parte de la Oficina Mexicana de Patentes relativa a combinaciones de iadademstat con inhibidores de PD-1 o PD-L1 para el tratamiento del cáncer. Una vez concedida formalmente, se espera que dicha patente proporcione protección al menos hasta 2040, excluyendo posibles extensiones de plazo de patente. Se han concedido o aprobado patentes correspondientes en Australia, Europa, Japón y Rusia.
Vafidemstat:
- Oryzon continúa con las actividades regulatorias y de desarrollo necesarias para respaldar el avance del ensayo PORTICO-2 de Fase III con vafidemstat en agresividad en trastorno límite de la personalidad (TLP). Tras la recepción de comentarios por escrito de la FDA relativos a los criterios de valoración del estudio y a determinadas consideraciones no clínicas, la Compañía está trabajando activamente en la generación de información adicional de soporte y en el refinamiento del protocolo requeridos para su nueva presentación. Estas actividades incluyen investigación cualitativa y trabajos de validación de criterios de valoración destinados a reforzar las escalas clínicas propuestas.
- Con el objetivo de seguir reforzando sus capacidades de desarrollo clínico en SNC, Oryzon nombró a Rolando Gutierrez-Esteinou, M.D., como Director Médico para programas de SNC. El Dr. Gutierrez-Esteinou es un psiquiatra formado en Harvard y un ejecutivo senior de desarrollo clínico con amplia experiencia en programas avanzados en neurociencias e interacciones regulatorias en indicaciones psiquiátricas.
- El reclutamiento continúa en el ensayo clínico de Fase IIb EVOLUTION que evalúa vafidemstat en esquizofrenia, centrado principalmente en síntomas negativos, con objetivos secundarios destinados a evaluar efectos sobre el deterioro cognitivo y los síntomas positivos. El estudio, llevado a cabo inicialmente en España, continúa su expansión a otros países europeos adicionales (Bulgaria, Polonia, Rumanía y Eslovaquia).
- Oryzon está finalizando los preparativos para el ensayo de Fase II HOPE-2 destinado a evaluar vafidemstat en agresividad asociada al trastorno del espectro autista (TEA). El ensayo se centrará en subpoblaciones de TEA definidas genéticamente, en particular en individuos con síndrome de Phelan-McDermid (PMS). El estudio se llevará a cabo inicialmente en España como parte de las actividades respaldadas por la iniciativa europea IPCEI Med4Cure.
- Oryzon también ha continuado reforzando su cartera de patentes para vafidemstat. La Compañía ha recibido recientemente una comunicación de “Decisión de concesión” por parte de la USPTO relativa a métodos para el tratamiento de síntomas no agresivos del TLP con inhibidores de LSD1 como vafidemstat. Una vez concedida, se espera que la patente estadounidense permanezca en vigor al menos hasta 2040, excluyendo posibles ajustes o extensiones del plazo de la patente. Se han concedido o aprobado patentes en esta familia también en Australia, Europa, Japón, México, Rusia, Singapur y Sudáfrica. Además, Oryzon recibió otra comunicación de “Decisión de concesión” de la Oficina Japonesa de Patentes relativa al uso de vafidemstat para el tratamiento de la agresividad y el aislamiento social. Se han concedido o aprobado patentes en esta familia también en Australia, Canadá, Europa, Hong Kong, Israel, Corea del Sur, Malasia, Filipinas y Rusia, y se espera que permanezcan en vigor al menos hasta 2038, excluyendo posibles extensiones del plazo de la patente.
Programas en fases más tempranas:
- ORY-4001, el inhibidor altamente selectivo de la histona deacetilasa 6 (HDAC6) de Oryzon para trastornos neurológicos, continúa avanzando en los estudios IND pre-regulatorios para preparar el compuesto para ensayos clínicos. El programa sigue centrado en potenciales aplicaciones en esclerosis lateral amiotrófica (ELA), enfermedad de Charcot-Marie-Tooth (CMT) y otros trastornos neurológicos.
Información financiera del primer trimestre de 2026
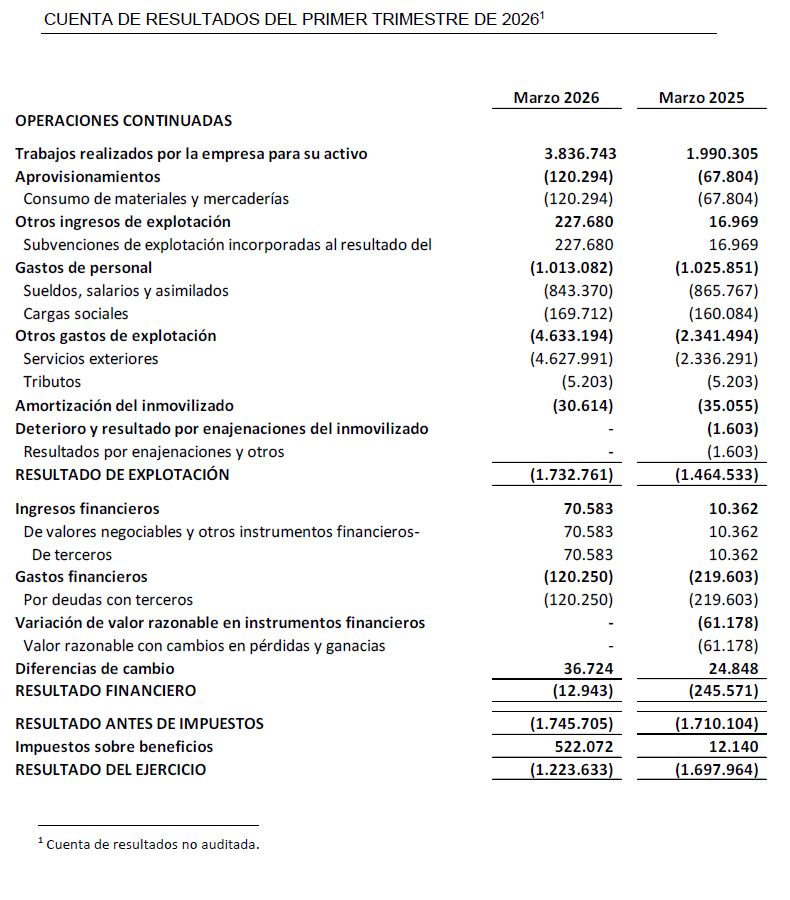
Significativo incremento del 88% de las inversiones en I+D a 31 de marzo de 2026 en comparación al primer trimestre del ejercicio 2025. Las inversiones en I+D han ascendido a 4,5 M€, de las cuales 4,2 M€ corresponden a actividades de desarrollo y 0,3 M€ a actividades de investigación.
El resultado neto al cierre del primer trimestre de 2026 se sitúa en -1,2 M€ frente al primer trimestre del ejercicio precedente de –1,7M€, lo que supone una mejora de 0,5M€ con respecto al cierre del primer trimestre del ejercicio precedente.
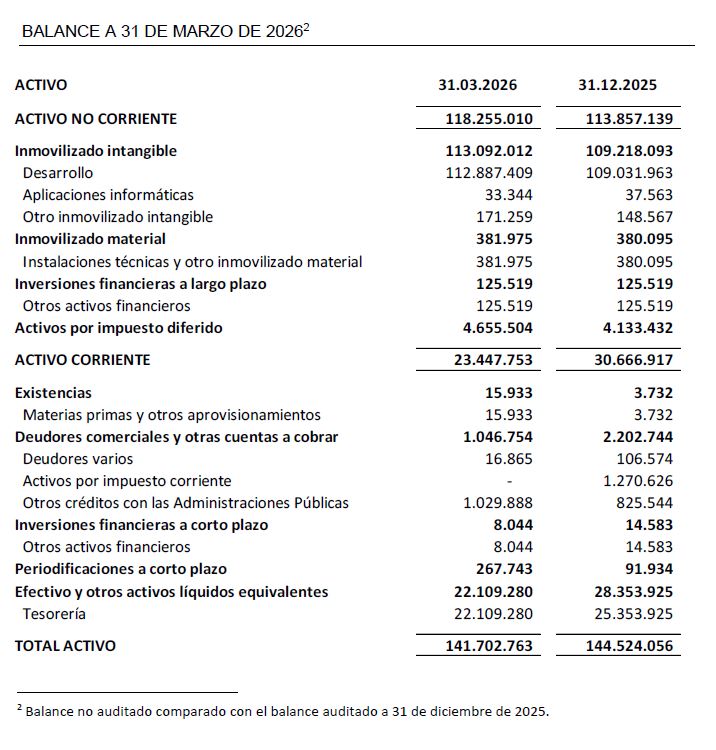
A 31 de marzo de 2026, Oryzon mantiene efectivo e inversiones financieras disponibles por importe de 22,1 M€.
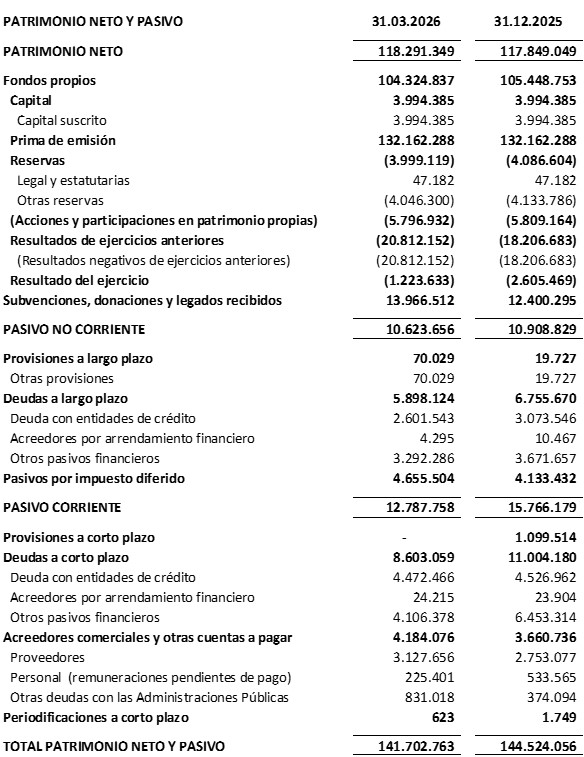
El balance a 31 de marzo de 2026 presenta un patrimonio neto de 118,3 M€.
En el pasivo corriente del balance, epígrafe otros pasivos financieros, se presentan 4,1 M€, de los cuales 3,5 M€ corresponden al reconocimiento de financiación anticipada relativa a la parte de subvención IPCEI que se encuentra pendiente de ejecución, y en su caso, su importe será traspasado a patrimonio neto en el momento de su ejecución.
Sobre Oryzon
Fundada en el año 2000 en Barcelona, España, Oryzon es una compañía biofarmacéutica de fase clínica y líder europea en epigenética, con un fuerte enfoque en medicina personalizada para enfermedades del sistema nervioso central (SNC) y oncología. El equipo de Oryzon está compuesto por profesionales altamente cualificados de la industria farmacéutica, con base en Barcelona, Boston y New Jersey. Oryzon tiene una cartera clínica avanzada, centrada en dos inhibidores de LSD1: iadademstat, su programa en oncología/hematología, con varios estudios en curso de Fase I y II y que ha mostrado resultados preliminares positivos en leucemia mieloide aguda (LMA), incluyendo una tasa de respuesta global (ORR) del 100% en LMA en primera línea; y vafidemstat, su programa principal en SNC, listo para Fase III en Trastorno Límite de la Personalidad. Además, la Compañía tiene otros programas dirigidos contra otras dianas epigenéticas, como HDAC6, donde ORY-4001 ha sido nombrado como candidato clínico para su potencial desarrollo para la enfermedad de Charcot–Marie–Tooth (CMT), esclerosis lateral amiotrófica (ELA) y otras enfermedades neurológicas. La compañía posee también una sólida plataforma para la identificación de biomarcadores y validación de dianas terapéuticas para una variedad de enfermedades oncológicas y neurológicas. Para más información, visitar www.oryzon.com
Sobre Iadademstat
Iadademstat (ORY-1001) es un inhibidor oral y altamente selectivo de la enzima epigenética LSD1, con un potente efecto diferenciador en cánceres hematológicos. Iadademstat ha mostrado resultados alentadores de seguridad y potente actividad clínica en combinación con azacitidina en un ensayo de Fase IIa en pacientes ancianos con LMA de primera línea (ensayo ALICE). Iadademstat está siendo evaluado actualmente en combinación con azacitidina y venetoclax en LMA en primera línea en un ensayo iniciado por investigador (IIS) esponsorizado por OHSU, y en combinación con gilteritinib en el ensayo de Fase Ib FRIDA esponsorizado por Oryzon en LMA refractaria/en recaida con mutaciones FLT3, con datos preliminares muy alentadores de seguridad y eficacia en ambos estudios: 100% de tasa de respuesta global (ORR) y 93% de tasa de remisión completa compuesta (CRc), con un79% de CR estrictas en LMA en 1L, y 67% CRc en LMA FLT3+ R/R . Estudios adicionales en marcha en hemato-oncología incluyen un ensayo IIS en síndrome mielodisplásico, y ensayos esponsorizados por el Instituto Nacional del Cáncer (NCI) de EEUU en neoplasias mieloproliferativas y en LMA en 1L, que se llevan a cabo en el marco del Acuerdo de Cooperación en Investigación y Desarrollo (CRADA) entre Oryzon y NCI. Más allá de los cánceres hematológicos, iadademstat está siendo evaluado en cáncer de pulmón de células pequeñas (CPCP) en estadío extenso en un ensayo de Fase I/II aleatorizado en primera línea en combinación con inhibidores de punto de control inmunitario (ICI) esponsorizado por el NCI y liderado por el Memorial Sloan Kettering Cancer Center, y en un ensayo IIS en combinación con ICI y radioterapia. Oryzon ha expandido también el desarrollo clínico de iadademstat a indicaciones hematológicas no oncológicas, con ensayos en anemia falciforme (estudio aprobado por la EMA, reclutando) y trombocitemia esencial (aprobado por la EMA). Iadademstat tiene la designación de medicamento huérfano para LMA en EEUU y la UE y para CPCP en EEUU.
Sobre Vafidemstat
Vafidemstat (ORY-2001) es un inhibidor de LSD1 optimizado para SNC activo por vía oral, con potencial para abordar trastornos neuropsiquiátricos mediante modulación epigenética. En estudios preclínicos, vafidemstat ha demostrado efectos sobre la cognición, la neuroinflamación, la agresividad y el comportamiento social, así como actividad neuroprotectora y antiinflamatoria en múltiples modelos de enfermedades del SNC. Oryzon ha completado varios ensayos clínicos de Fase II con vafidemstat, incluidos los estudios REIMAGINE y REIMAGINE-AD en agresividad en pacientes con distintos trastornos psiquiátricos y en pacientes agitados/agresivos con Enfermedad de Alzheimer moderada o grave, respectivamente, con resultados clínicos positivos reportados en ambos ensayos. Tras completar el ensayo global aleatorizado, doble ciego, de Fase IIb PORTICO en trastorno límite de la personalidad (TLP), vafidemstat está avanzando como activo listo para Fase III en agitación/agresividad en TLP (Fase III en preparación). Vafidemstat también está siendo evaluado en el ensayo en curso de Fase IIb EVOLUTION, doble ciego, aleatorizado y controlado con placebo, en síntomas negativos de la esquizofrenia. Además, Oryzon está desplegando un enfoque de medicina de precisión en SNC con vafidemstat en subpoblaciones de pacientes genéticamente definidas en ciertas enfermedades del SNC, así como en síndromes del neurodesarrollo, incluyendo los preparativos para un nuevo ensayo clínico en agresividad en pacientes con trastornos autistas como el síndrome de Phelan-McDermid.
AFIRMACIONES O DECLARACIONES CON PROYECCIONES DE FUTURO
Esta comunicación contiene información y afirmaciones o declaraciones con proyecciones de futuro sobre Oryzon. Asimismo, incluye proyecciones y estimaciones financieras con sus presunciones subyacentes, declaraciones relativas a planes, objetivos, y expectativas en relación con futuras operaciones, inversiones, sinergias, productos y servicios, y declaraciones sobre resultados futuros. Las declaraciones con proyecciones de futuro no constituyen hechos históricos y se identifican generalmente por el uso de términos como “espera”, “anticipa”, “cree”, “pretende”, “estima” y expresiones similares.
Si bien Oryzon considera que las expectativas recogidas en tales afirmaciones son razonables, se advierte a los inversores y accionistas de Oryzon de que la información y las afirmaciones con proyecciones de futuro están sometidas a riesgos e incertidumbres, muchos de los cuales son difíciles de prever y están, de manera general, fuera del control de Oryzon, lo que podría provocar que los resultados y desarrollos reales difieran significativamente de aquellos expresados, implícitos o proyectados en la información y afirmaciones con proyecciones de futuro. Entre tales riesgos e incertidumbres están aquellos identificados en los documentos remitidos por Oryzon a la Comisión Nacional del Mercado de Valores y que son accesibles al público.
Se recomienda no tomar decisiones sobre la base de afirmaciones o declaraciones con proyecciones de futuro, ya que se refieren exclusivamente a la fecha en la que se manifestaron, no constituyen garantía alguna de resultados futuros y no han sido revisadas por los auditores de Oryzon. La totalidad de las declaraciones o afirmaciones de futuro de forma oral o escrita emitidas por Oryzon o cualquiera de sus miembros del consejo, directivos, empleados o representantes quedan sujetas, expresamente, a las advertencias realizadas. Las afirmaciones o declaraciones con proyecciones de futuro incluidas en este documento están basadas en la información a disposición de Oryzon a la fecha de esta comunicación.